Les chercheurs de Johns Hopkins (Baltimore) ont découvert que les faibles niveaux de cuivre cellulaire semblaient rendre les cellules adipeuses plus grosses en modifiant la façon dont elles traitent leurs principaux combustibles métaboliques, tels que le sucre et les graisses. Ainsi, des cellules adipeuses déficientes en cuivre vont doubler de taille par rapport à des adipocytes normaux. Ces travaux, présentés dans la revue PLoS Biology, désignent une enzyme clé, la “semicarbazide-sensitive amine oxidase” ou SSAO, qui apparaît donc à des niveaux extrêmement élevés dans les adipocytes et se révèle ainsi une cible prometteuse.
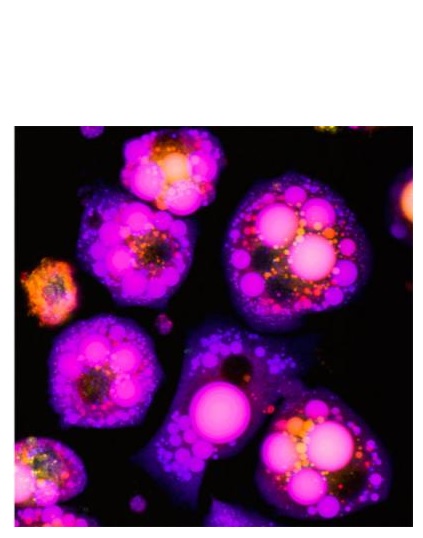
La protéine SSAO, présente dans la membrane cellulaire exerce une activité enzymatique qui génère notamment la formation d’hydrogène peroxyde, un composé qui participe au stress oxydatif cellulaire. Dans le cadre de cette étude menée sur des cellules de souris, les chercheurs du Johns Hopkins constatent que le faible taux de cuivre dans les cellules rend les cellules adipeuses plus grosses (Visuel 2). Le faible niveau de cuivre semble modifier la façon dont les cellules métabolisent le sucre et les graisses.
L'homéostasie du cuivre, une cible thérapeutique pour les troubles métaboliques, dont l'obésité ? C’est bien l’hypothèse documentée ici, alors que des liens entre le cuivre et l'obésité ont déjà été suggérés par de précédentes études chez l'Homme. En Occident, les carences alimentaires en cuivre ne sont pas courantes, sauf pendant la grossesse, et un régime comportant des légumes, des noix et du chocolat suffit généralement à maintenir les niveaux de cuivre nécessaires à la santé. Le rôle du cuivre est largement documenté : il contribue à de nombreux processus, de la formation de pigments dans la couleur des cheveux et des yeux à l’angiogenèse et aux processus cognitifs. Ainsi, des déséquilibres en cuivre ont déjà été associés à plusieurs troubles neurologiques : « nous avons constaté maintes et maintes fois que lorsqu'un tissu présente un déséquilibre en cuivre, il en résulte des effets importants sur sa santé », ajoute le Dr Svetlana Lutsenko, professeur de physiologie à la Johns Hopkins University.
Cuivre et adipocytes : les travaux décrivent ici le rôle de l'équilibre du cuivre dans la physiologie des cellules adipeuses ou adipocytes. Les chercheurs ont cultivé en laboratoire des précurseurs de cellules adipeuses de souris amenés à se transformer en adipocytes matures et ont surveillé l'absorption de cuivre par les cellules et identifié les protéines produites par les cellules au cours de leur développement. Ils constatent ainsi que, pendant la maturation, les adipocytes ingèrent deux fois plus de cuivre que les précurseurs et que plusieurs protéines contenant du cuivre sont plus abondantes, en particulier l’enzyme SSAO, extraordinairement régulée à la hausse, jusqu’à des niveaux 70 fois plus élevés que dans les cellules précurseurs.
Pour vérifier si la consommation de cuivre des cellules affecte la fonction de SSAO, les scientifiques ont limité la disponibilité en cuivre pendant la maturation des adipocytes. Ils constatent que le manque de cuivre n'empêche pas les cellules de se développer en cellules adipeuses matures, mais que les cellules privées de cuivre ont une taille 2 fois supérieure à celle de leurs homologues saines. De plus ces cellules contiennent plus de molécules de lipides.
Le cuivre est donc un facteur clé dans le développement et le métabolisme sains des adipocytes.
SSAO et adipocytes : les chercheurs démontrent ensuite que les cellules privées de SSAO se comportent comme les cellules privées de cuivre : lorsqu'elles sont chimiquement induites à devenir des cellules adipeuses matures, ces cellules ressemblent exactement aux cellules dépourvues de cuivre des expériences précédentes : leur taille est environ 2 fois supérieure à celle des cellules normales et elles contiennent également plus de lipides.
Cuivre, SSAO et accumulation de graisse : ensemble, ces données confirment que les niveaux de cuivre cellulaire sont essentiels à la fonction de SSAO et que l'inactivation de cette enzyme entraîne une croissance anormale des cellules adipeuses. En fait, il s’avère que ces cellules accumulent alors plus de lipides, ce qui, concrètement aboutit à une accumulation de graisse. D’autres expériences montrent que SSAO régule 200 protéines toutes impliquées dans 17 voies cellulaires régulant le métabolisme. En cas d’absence de SSAO, les principales modifications sont justement observées au niveau des protéines qui absorbent et transforment le sucre, et les protéines qui qui absorbent et transforment les lipides…SSAO se révèle au bout du compte une enzyme vitale pour de nombreuses fonctions métaboliques.
D’autres recherches vont donc être menées sur l’enzyme SSAO, en particulier chez des patients souffrant de stéatose hépatique et de diabète, car dans ces cas, SSAO apparaît à des niveaux sanguins particulièrement élevés.
SSAO apparait donc comme une cible clé dans la régulation énergétique et cellulaire.
Source: PLOS Biology September 10, 2018 DOI : 10.1371/journal.pbio.2006519 Copper-dependent amino oxidase 3 governs selection of metabolic fuels in adipocytes (Visuel 2 Haojun Yang, Johns Hopkins Medicine)
Plus sur Obésité Blog
